Explorando os mistérios da Tabela Periódica
A Tabela Periódica é uma das ferramentas mais importantes da química, ela é capaz de desvendar mistérios e trazer soluções para diversas áreas de conhecimento. Ao estudar a tabela, é possível conhecer as propriedades e características de cada elemento químico, assim como suas ligações e reações. Dessa forma, o estudo da tabela periódica é fundamental para a compreensão da química.
Desvendando a magia dos elementos químicos na Tabela Periódica
Cada elemento químico traz consigo uma magia única, e a Tabela Periódica é a chave para desvendá-la. Cada elemento possui suas próprias propriedades, que determinam como ele se comporta em diferentes situações. Por exemplo, o hidrogênio é o elemento mais abundante do universo e é fundamental para a vida no planeta Terra, já o ouro é um metal precioso e muito valioso na sociedade atual.
Ao estudar a Tabela Periódica, é possível entender a relação entre os elementos químicos e as suas propriedades. Os elementos são organizados de acordo com o número atômico, que determina o número de prótons presentes no núcleo do átomo. A organização da tabela permite a visualização das propriedades periódicas dos elementos, como eletronegatividade, potencial de ionização e raio atômico. Essas informações são essenciais para a compreensão da química e para a utilização dos elementos em diversas aplicações.
A Tabela Periódica é uma fonte inesgotável de conhecimento e inspiração. Ela é a base para a compreensão da química e é fundamental para a criação de novos materiais e tecnologias. Ao estudar os elementos químicos e suas propriedades, é possível desvendar mistérios e criar soluções para os mais diversos problemas. A ciência é fascinante, e a Tabela Periódica é um dos seus maiores tesouros.
A Tabela Periódica é uma ferramenta incrível que nos permite explorar a magia dos elementos químicos. Ao compreender as propriedades e características de cada elemento, podemos criar novas tecnologias e soluções para os mais diversos problemas. A ciência é uma fonte inesgotável de conhecimento, e a Tabela Periódica é uma das suas maiores riquezas. Continue explorando os mistérios da química e descubra a fascinante magia dos elementos!
1. (Unesp 2023)
O alumínio é um metal valorizado por ter baixa densidade e baixa temperatura de fusão, o que o torna ideal para a fabricação de embalagens baratas, resistentes e de fácil reciclagem, além de amplo uso na fabricação de veículos. O gráfico mostra um comparativo de cinco metais, incluindo o alumínio, para cinco propriedades.
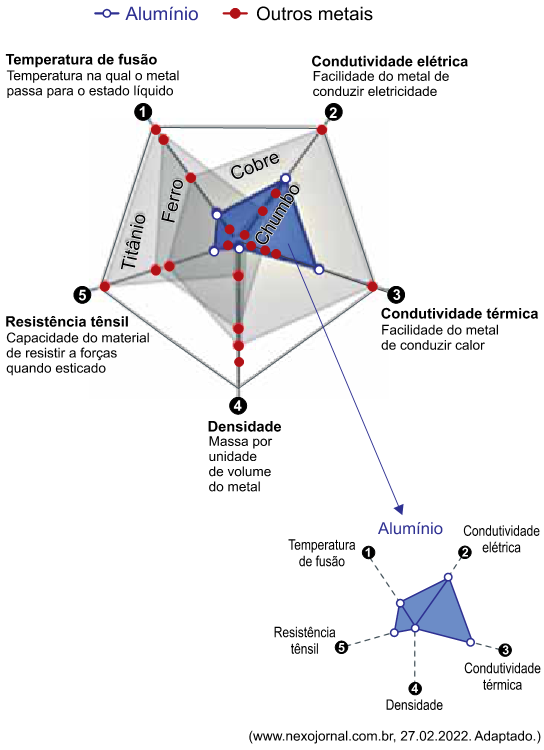
Considerando-se que em determinado projeto industrial são desejáveis os menores valores possíveis das propriedades 1 e 4 e os maiores valores possíveis das propriedades 2, 3 e 5, dos cinco metais comparados, o alumínio é o mais vantajoso
a) nas propriedades 1 e 4, apenas.
b) nas propriedades 3 e 4, apenas.
c) na propriedade 4, apenas.
d) na propriedade 1, apenas.
e) na propriedade 3, apenas.
2. (Ita 2023)
Considere as seguintes afirmações relacionadas a átomos e íons atômicos no estado gasoso:
I. A afinidade eletrônica do átomo de oxigênio é maior do que a do ânion O−.
II. A energia de ionização do átomo de oxigênio é maior do que a do ânion O2−.
III. O raio atômico do átomo de oxigênio é maior do que o do ânion O−.
IV.O átomo de oxigênio tem maior afinidade eletrônica e menor energia de ionização do que o átomo de nitrogênio.
Das afirmações I a IV, acima destacadas, são CORRETAS
a) apenas I e II.
- b) apenas I, II e IV.
- c) apenas I e III.
- d) penas II, III e IV.
- e) apenas III e IV.
3. (Ita 2023)
Considere que valores maiores de energia de hidratação são observados para íons com menor tamanho e maior carga. Com base nessa informação, são feitas as seguintes comparações entre a energia de hidratação dos pares de íons abaixo.
- I. Li+ > K+.
II. B3+ > Al3+.
III. Sr2+ < Ca2+.
- IV. Ga3+ > Ca2+.
V. S2− > Se2−.
Das comparações I a V, acima destacadas, são CORRETAS
- a) apenas I e II.
- b) apenas I, II e IV.
- c) apenas II, III e V.
- d) apenas III, IV e V.
- e) todas.
4. (Uece 2023)
Na comparação entre as famílias dos halogênios e dos metais alcalinos, os halogênios apresentam valores mais altos de
a) poder redutor.
b) ponto de fusão.
c) afinidade eletrônica.
d) densidade.
Gabarito – Vestibular 2023
Questão 1: C
Questão 2: B
Questão 3: E
Questão 4: C
Sugestão de vídeos:



